Instrukcje dla nauczyciela do symulacji PhET - Oddziaływanie atomów
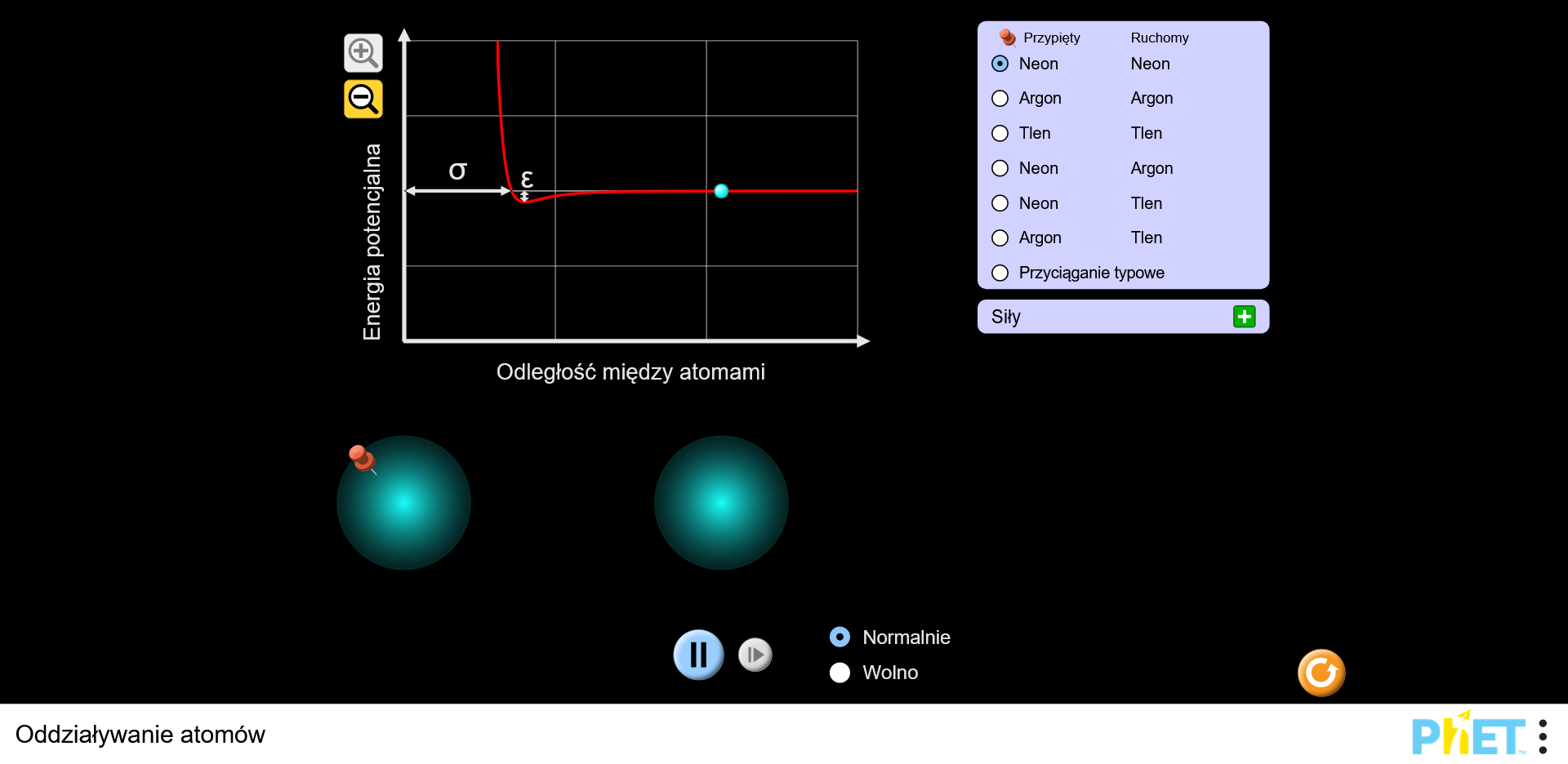
W symulacji Oddziaływanie atomów uczniowie badają, w jaki sposób siły przyciągania i odpychania zależą od odległości między atomami.
PhET Interactive Simulations, University of Colorado Boulder, https://phet.colorado.edu Na licencji CC BY 4.0
W opracowaniu niniejszego poradnika wykorzystano materiały PhET: Strona źródłowa symulacji, Teacher Tips (Rouinfar, sierpień 2023)
W szablonie strony wykorzystano kod html/css: phydemo.app.
Szkoła średnia
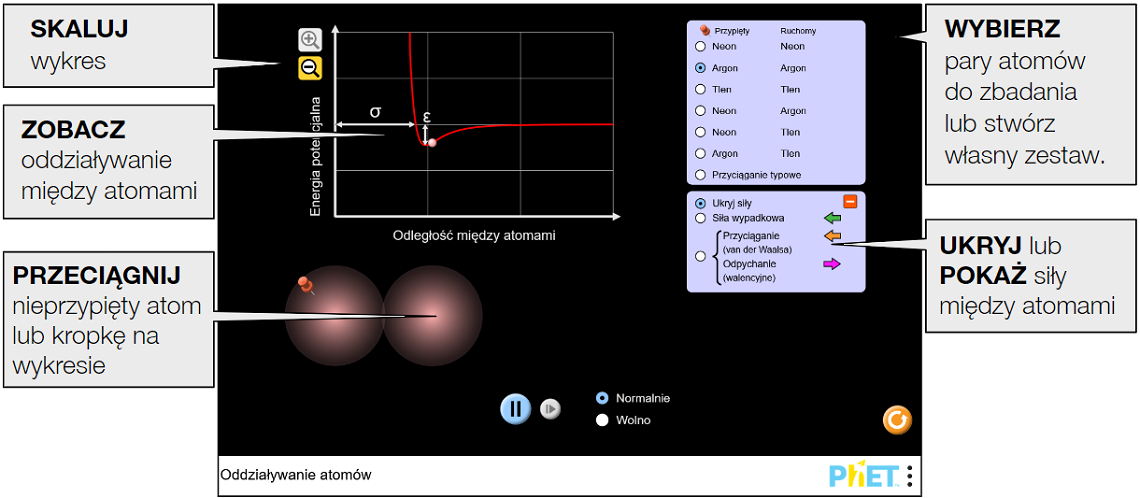
Zapoznaj się z oddziaływaniami pomiędzy różnymi atomami. Włącz strzałki pokazujące siły, aby zobaczyć zarówno wypadkowe siły działające na atomy, jak również siły przyciągania i odpychania.
Poniższe parametry query umożliwiają dostosowanie symulacji i można je dodać, dołączając znak '?' do adresu URL symulacji i oddzielając każdy parametr query znakiem '&'. Ogólny wzorzec adresu URL to: …html?queryParameter1&queryParameter2&queryParameter3
Na przykład, jeśli w aplikacji Oddziaływanie atomów chcesz włączyć tryb projektora (colorProfile=projector), z wyłączonymi linkami zewnętrznymi (allowLinks=false), użyj: https://www.edukator.pl/tik_edukator/atomic-interactions_all.html?colorProfile=projector&allowLinks=false
Aby uruchomić to w języku polskim (locale=pl), adres URL będzie wyglądał następująco: https://www.edukator.pl/tik_edukator/atomic-interactions_all.html?locale=pl&colorProfile=projector&allowLinks=false

Wskazuje, że dostęp do tego dostosowania można uzyskać też z menu Preferencje lub Opcje... w symulacji.
| Parametr query i opis | Przykłady |
| locale - określa język symulacji przy użyciu kodów ISO 639-1. Dostępne wersje językowe można znaleźć na stronie symulacji w zakładce Tłumaczenia. Uwaga: działa to tylko wtedy, gdy adres URL symulacji kończy się na “_all.html”. | locale=pl (polski) locale=fr (francuski) |
 colorProfile - zmienia kolory symulacji dla łatwiejszej projekcji. colorProfile - zmienia kolory symulacji dla łatwiejszej projekcji. | colorProfile=projector |
| allowLinks - jeśli false, wyłącza linki, które prowadzą uczniów do zewnętrznego adresu URL. Domyślnie jest true. | allowLinks=false |

Po kliknięciu logo PhET (na dole po prawej) pojawia się okno zawierające informacje dotyczące symulacji. Możemy tu zmienić sposób jej wyświetlania.
Klikając Pełny ekran przechodzimy do trybu pełnoekranowego (powrót - klawisz escape).
Klikając Opcje… w pojawiającym się oknie możemy zaznaczyć Tryb projektora, aby ułatwić projekcję. Następuje wtedy odwrócenie kolorów, tak jak na zrzucie ekranu poniżej.
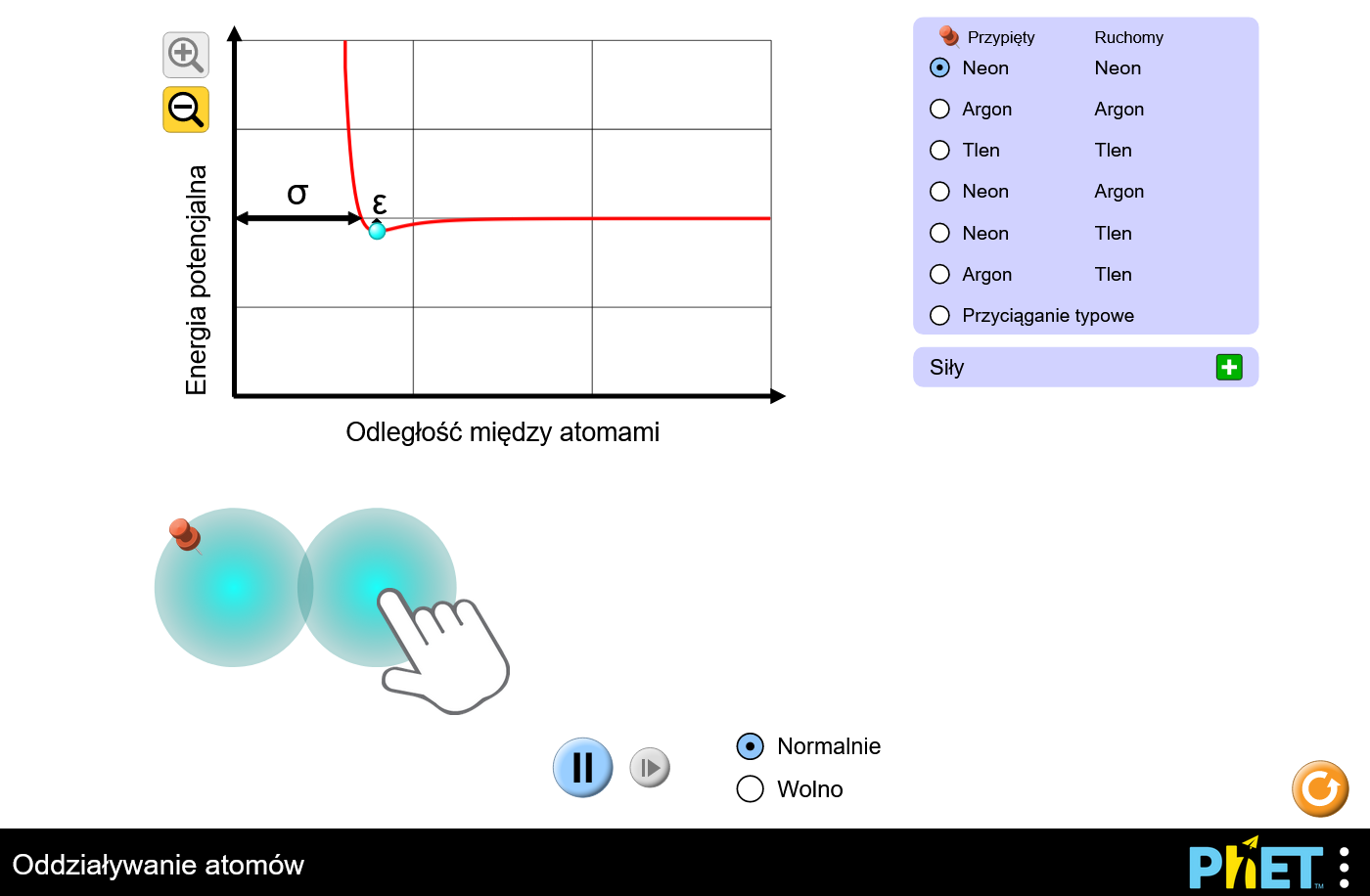
Dostępne są również wersje symulacji niewymagające połączenia z internetem.
Aplikacja PhET Desktop zawiera wszystkie symulacje HTML5 i Java, w tym ich tłumaczenia, do użytku offline w systemach Windows i macOS (dostępne po zalogowaniu tu). Symulacje HTML5 nie wymagają dodatkowego oprogramowania, natomiast do uruchamiania dowolnych symulacji Java w aplikacji komputerowej jest wymagany Java SE Development Kit 8.
Za symboliczną opłatą możemy pobrać w postaci jednej aplikacji wszystkie materiały PhET, które zostały opublikowane w html5. Telefony, tablety i Chromebooki (z systemem Android): Google Play. iPhone'y i iPady (aplikacja na iOS): App Store
Darmową wersję desktopową tej aplikacji pobierzemy bezpośrednio klikając tu - wersja _pl zawiera polską (domyślną) i angielską wersję językową i tu - wersja _all zawiera angielską (domyślną) i wszystkie inne dostępne wersje językowe lub ze strony PhET (klikając przycisk ze strzałką przy wybranej wersji językowej):

Wskazówki dotyczące wszystkich symulacji zawarte są w informacjach ogólnych.
Więcej porad dotyczących korzystania z symulacji z uczniami można znaleźć na stronach PhET w sekcji Wskazówki dotyczące korzystania z PhET.
Zobacz wszystkie opublikowane na stronach PhET aktywności dla Oddziaływanie atomów tutaj (dostęp do materiałów wymaga zalogowania).