Zagadnienia
- Mechanika kwantowa
- Atom wodoru
- Model Bohra
- Długość fali DeBroglie'a
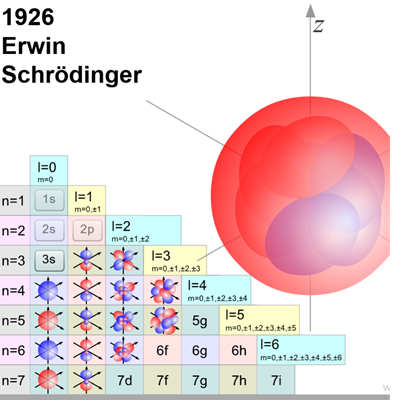
- Model Schrödingera
Opis
W tej symulacji użytkownik najpierw obserwuje symulowane widmo światła wodoru. Po zbadaniu widmo to można porównać z wynikami przewidywanymi przez różne modele atomu (Johna Daltona, J.J. Thomsona, Ernesta Rutherforda, Nielsa Bohra, Louisa de Broglie i Erwina Schrödingera).
Źródło: OpenStax GitHub, na licencji GNU Affero General Public License Version 3.0 (na podstawie PhET Interactive Simulations, University of Colorado Boulder, https://phet.colorado.edu Na licencji CC BY 4.0).
W opracowaniu niniejszego poradnika wykorzystano materiały PhET: Strona źródłowa symulacji, Teacher Tips (Sam McKagan, wrzesień 2012)
W szablonie strony wykorzystano kod html/css: phydemo.app.
Poziom
Szkoła podstawowa, szkoła średnia
Przykładowe cele nauczania
- Zwizualizuj różne modele atomu wodoru.
- Wyjaśnij, jakie eksperymentalne przewidywania zawiera każdy z modeli.
- Wyjaśnij, dlaczego ludzie wierzyli w poszczególne modele i dlaczego każdy historyczny model był niedoskonały.
- Wyjaśnij związek między fizycznym obrazem orbitali a diagramem poziomu energetycznego elektronu.
Przykładowe materiały teoretyczne
- Budowa atomu wodoru. Stan podstawowy i stany wzbudzone (ZPE)
- Współczesny opis budowy atomu (ZPE)
- W jaki sposób możemy zinterpretować linie widmowe? (ZPE)
- Czym są widma emisyjne? (ZPE)
- Obserwacja widm atomowych za pomocą siatki dyfrakcyjnej (ZPE)
- Powstawanie widm emisyjnych na przykładzie atomu wodoru (ZPE)
- Model atomu wodoru Bohra (OpenStax)
- Budowa atomu (OpenStax)
- Model atomu Bohra (Khan Academy)
Sterowanie symulacją
Jak naukowcy odkryli strukturę atomów bez patrzenia na nie? Wypróbuj różne modele, strzelając światłem w atom. Sprawdź, czy prognozy wynikające z modelu odpowiadają wynikom eksperymentalnym.
Ekran symulacji
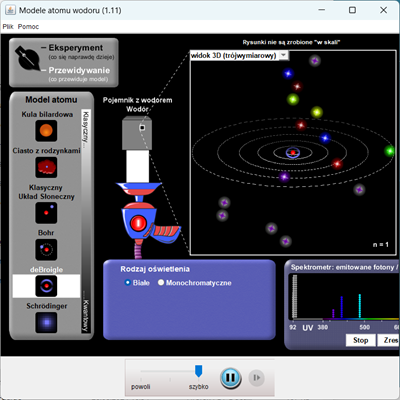
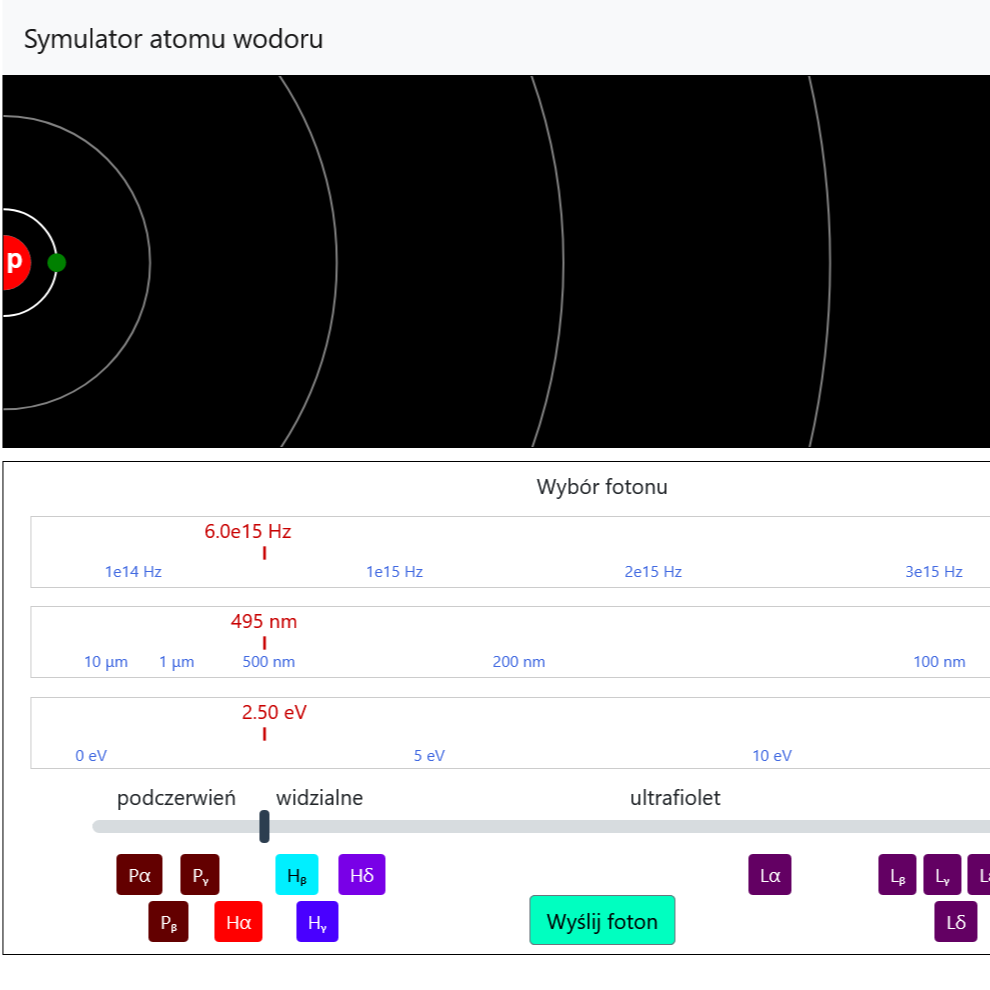
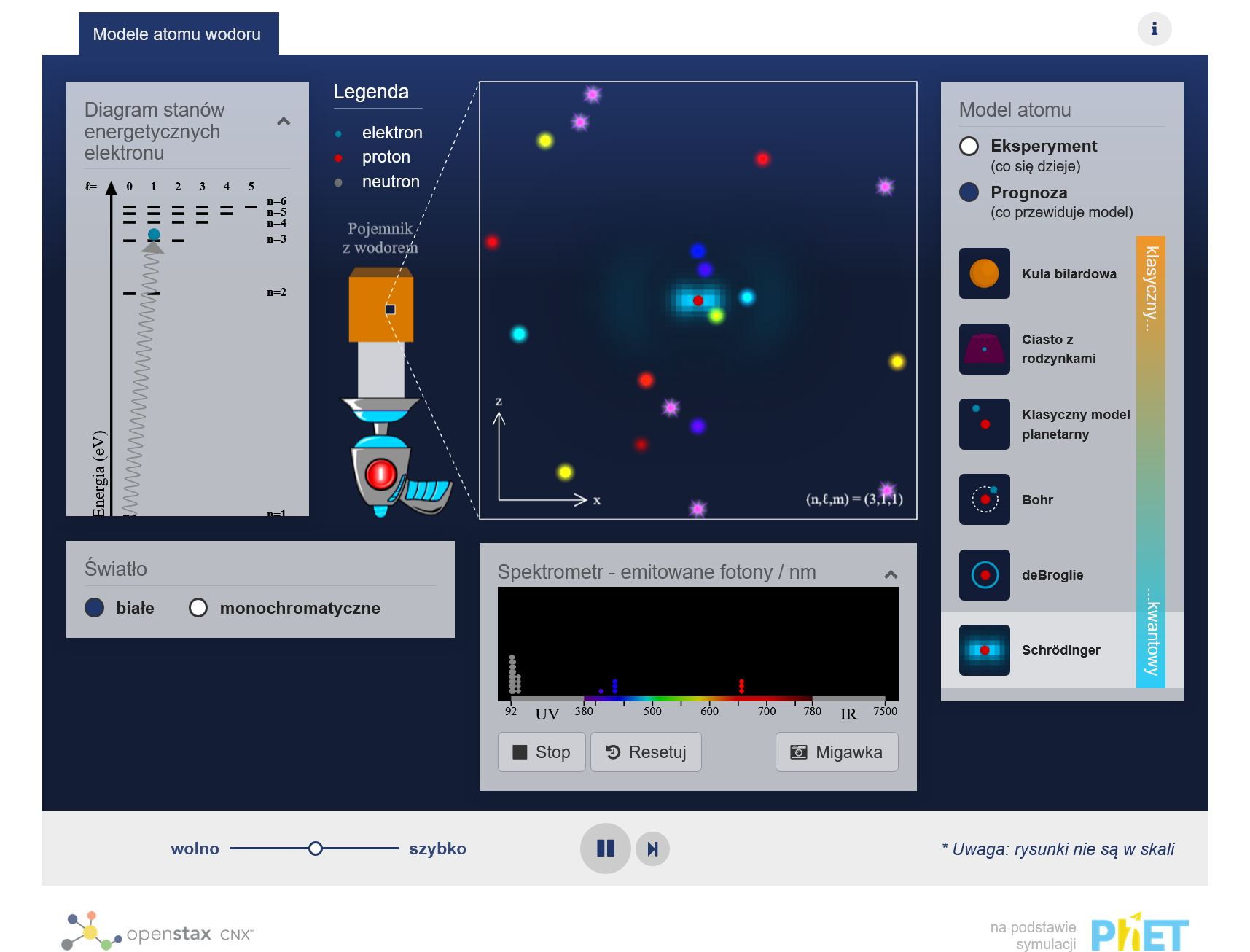
Zapoznaj się z wynikami eksperymentu - obserwuj widmo światła wysyłanego przez wodór pobudzony do świecenia, a następnie porównaj je z wizualizacjami prognoz wynikających z różnych modeli atomu.
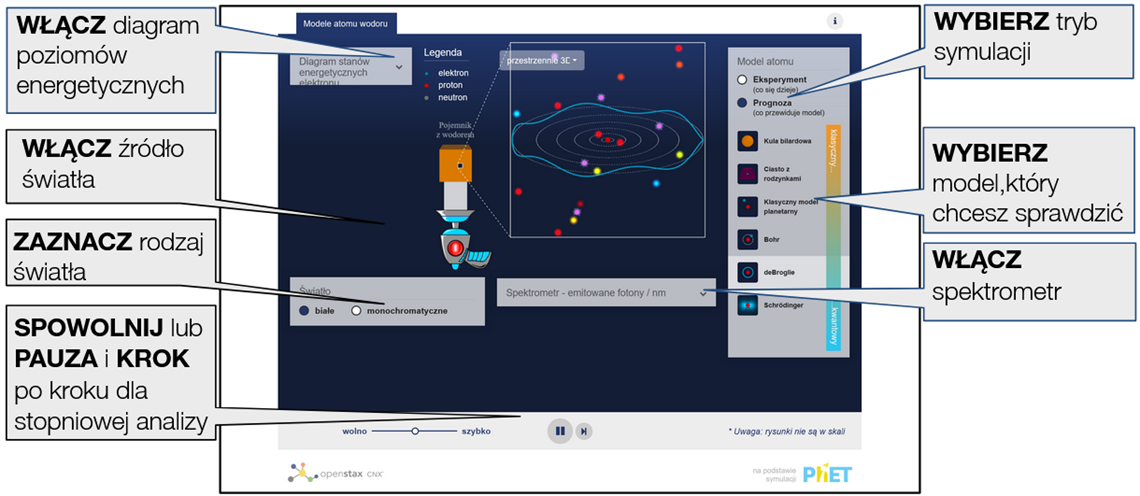
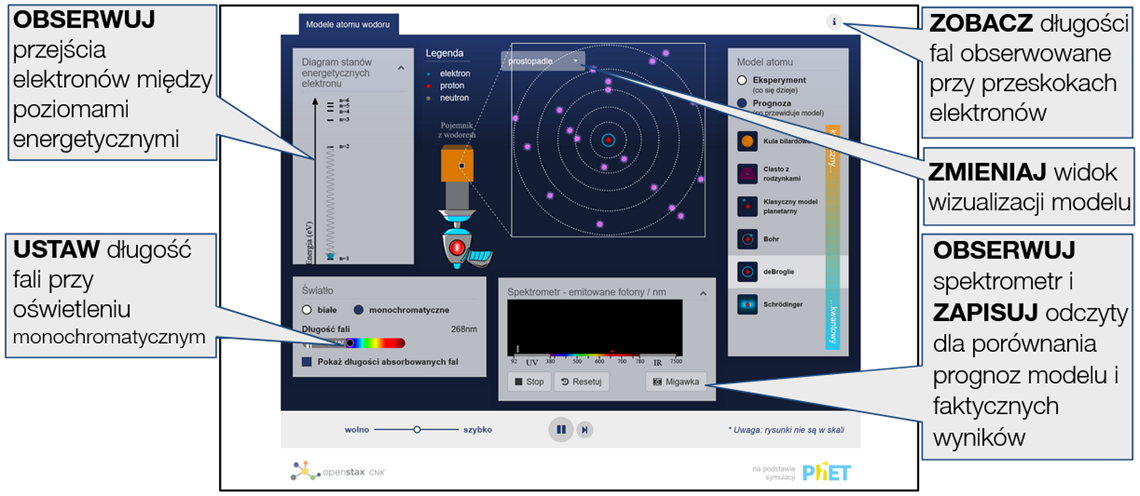
Złożone sterowanie
- W trybie Eksperyment pojedynczy atom wodoru jest ukryty w czarnej skrzynce. W trybie Prognoza atom jest widoczny. Uczniowie powinni być w stanie odkryć, że tylko przewidywania modelu Schrodingera są zgodne z wynikami eksperymentu.
- Wybierz opcję Przejścia, klikając na górze po prawej kółko z literą i, aby wyświetlić długości fal wymagane dla przejść w modelach Bohra, deBroglie'a i Schrödingera. Jeśli opcja Rodzaj oświetlenia jest ustawiona na Monochromatyczne, suwak długości fali miga na biało, gdy przekracza długość fali, która może wzbudzić elektron ze stanu podstawowego.
- Użyj ikony aparatu
 , aby wykonać migawkę spektrometru w celu porównania wyników dla różnych modeli.
, aby wykonać migawkę spektrometru w celu porównania wyników dla różnych modeli.
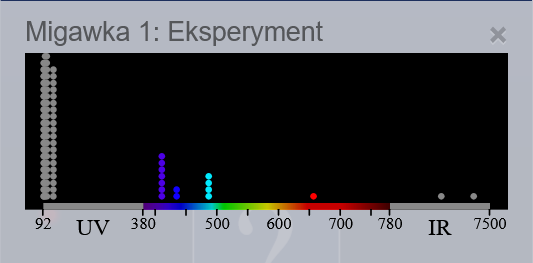
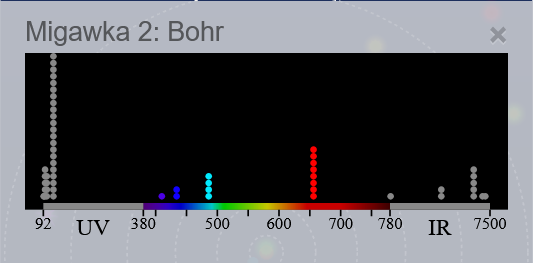
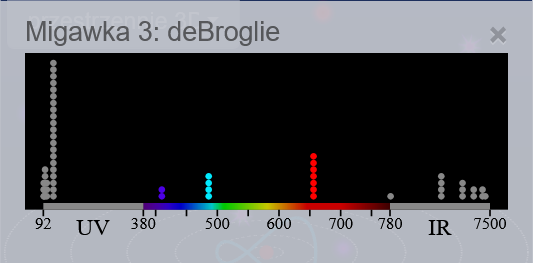
- Ustaw suwak na dole na szybko, aby szybko uzyskać wynik rejestrowanych przez spektrometr fotonów.
- Można wstrzymać symulację, a następnie użyć funkcji Krok, aby przeprowadzić stopniową analizę.
Spostrzeżenia na temat korzystania z aplikacji przez uczniów
- Uczniowie mogą nie zdawać sobie sprawy, że fotony UV mogą mieć różne długości fal, ponieważ wszystkie wyglądają tak samo (wyświetlane są na szaro).
- Jeśli opcja Rodzaj oświetlenia jest ustawiona na Monochromatyczne, uczniowie mogą nie zdawać sobie sprawy, że muszą przesunąć suwak do obszaru UV, aby wzbudzić atomy.
- Wielu uczniów ma problemy z identyfikacją czerwonej substancji w modelu ciasto z rodzynkami jako ładunku dodatniego. W wywiadach widzimy, że niektórzy uczniowie opisują ten model jako chmurę ujemnego ładunku wypełnioną małymi drobinkami ładunku dodatniego, a nie odwrotnie. Słowo chmura sugeruje, że mylą oni model ciasta z rodzynkami z modelem Schrödingera, w którym elektrony są często opisywane jako chmura ładunku ujemnego. Uczniowie ci początkowo myśleli, że elektron w symulacji to proton, ale ostatecznie byli w stanie poprawnie go zidentyfikować, korzystając z legendy lub porównując go z elektronami w innych modelach.
Uproszczenia / założenia modelu
- Atomy nie są w skali!
- W modelu Schrödingera przejścia podlegają regułom selekcji ∆l = ±1, ∆m = 0,±1. Z powodu tych reguł selekcji, stan 2,0,0 jest stanem metastabilnym, z którego elektron nie może spontanicznie wyemitować fotonu. Jeśli światło jest ustawione na białe, za każdym razem, gdy elektron znajdzie się w tym stanie, działo wkrótce wyemituje foton o dokładnie odpowiedniej energii, aby go wzbudzić. Jeśli światło jest ustawione na monochromatyczne, elektron pozostanie w tym stanie, chyba że wybierzesz długość fali, która może go z niego wzbudzić.
- W modelach Bohra i deBroglie'a przejścia między dowolnymi dwoma poziomami są równie prawdopodobne. W modelu Schrödingera prawdopodobieństwo przejścia opiera się na nakładaniu się funkcji falowych, a niektóre przejścia są zabronione lub wysoce nieprawdopodobne. Dlatego też w modelu Schrödingera występuje mniej linii widmowych niż w modelu Bohra lub deBroglie'a.
- W modelu Thomsona, zwanym także modelem ciasta z rodzynkami, zakładamy, że elektron może absorbować światło o dowolnej częstotliwości, ale zawsze emituje światło o częstotliwości równej jego częstotliwości oscylacji.
Sugestie dotyczące wykorzystania
Wskazówki dotyczące wszystkich symulacji zawarte są w informacjach ogólnych.
Więcej porad dotyczących korzystania z symulacji z uczniami można znaleźć na stronach PhET w sekcji Wskazówki dotyczące korzystania z PhET.
- Poproś uczniów o określenie, który model najbardziej odpowiada obserwacjom eksperymentalnym.
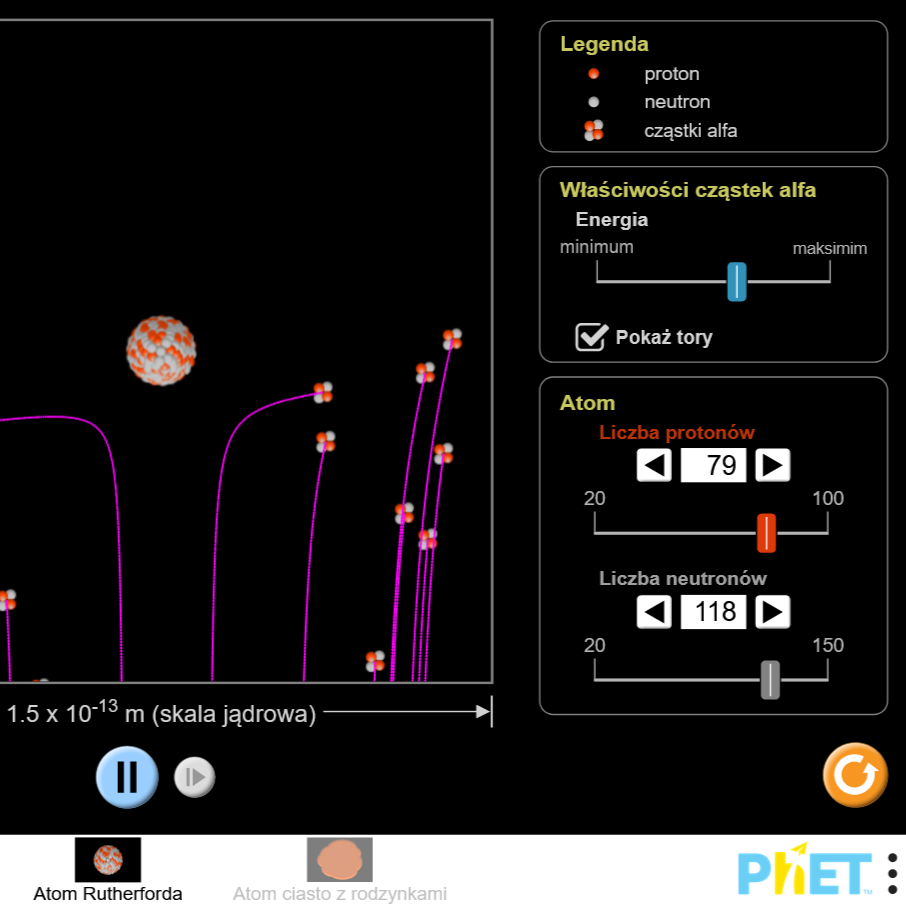
- Poproś uczniów, aby wyjaśnili powody, dla których ludzie uznawali każdy model, a także powody, dla których odrzucali każdy kolejny na rzecz nowego. Ta symulacja może być używana w połączeniu z symulacją Doświadczenie Rutherforda, która ilustruje powody przejścia od modelu ciasta z rodzynkami do modelu układu słonecznego.
Przykładowe polecenia
- Włącz wiązkę światła białego i wybierz tryb Eksperyment. Obserwuj, co się dzieje, gdy fotony są przesyłane przez atom wodoru. Opisz swoje obserwacje
- Jak myślisz, co sprawia, że fotony się odchylają? Co zaobserwowałeś na temat tego, ile lub jakiego koloru fotony są odchylane?
- Zmień ustawienie opcji Światło z Białe na Monochromatyczne. Koniecznie przetestuj różne długości fali, przesuwając suwak. Jakie są podobieństwa i różnice w zachowaniu fotonów?
- Kliknij pole Spektrometr - emitowane fotony. Zmień kolory fotonów na sugerowane, pozwól symulacji działać przez kilka minut, a następnie zapisz obserwacje.
- Zaznacz przycisk Prognoza i obserwuj konsekwencje różnych hipotez dotyczących atomu. Dokonuj porównań, używając długości fali 97 nm i białego światła. Porównuj dane doświadczalne w Eksperyment z przewidywaniami wynikającymi z danej hipotezy w Prognoza.
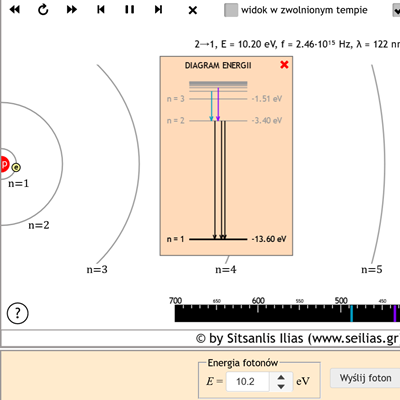
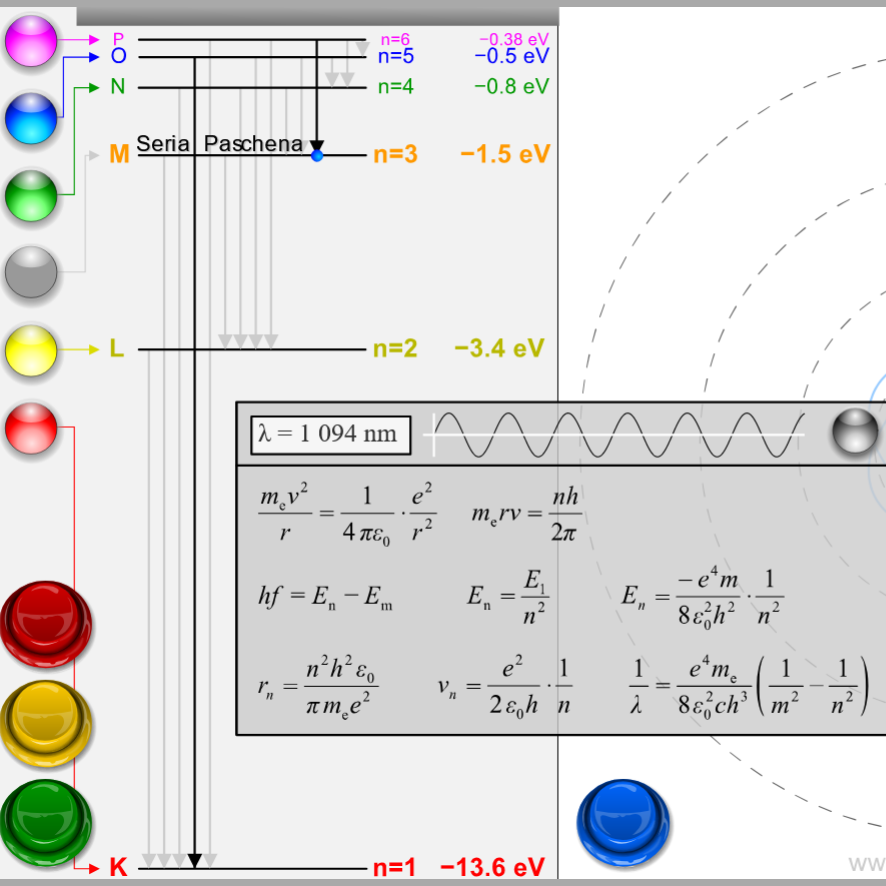
- Po wybraniu modelu Bohra rozwiń Diagram stanów energetycznych elektronu. Używając diagramu poziomów energii elektronów i spektrometru, opisz, co dzieje się z elektronem wodoru.
- Na górze po prawej kliknij kliknij kółko z literą i - Przejścia. Ustaw kolejno pierwsze 5 długości fal i obserwuj, co dzieje się z elektronem. Czy to potwierdza Twoje pomysły z poprzedniego punktu? Jeśli nie, zmień swoje stwierdzenie, aby przedstawić nowe koncepcje dotyczące zachowania elektronu.
- Teraz wprowadź długości fal, które nie są wymienione. Co obserwujesz? Czy to potwierdza twoje pomysły? Jeśli nie, dostosuj swoje stwierdzenie, aby wyjaśnić nowe zachowanie elektronu.
Zobacz wszystkie opublikowane na stronach PhET aktywności dla Modele atomu wodoru tutaj (dostęp do materiałów wymaga zalogowania).
Symulacje zbliżone tematycznie


 , aby wykonać migawkę spektrometru w celu porównania wyników dla różnych modeli.
, aby wykonać migawkę spektrometru w celu porównania wyników dla różnych modeli.